tDCS در درمان درد
تحلیل وضعیت و مسیرهای آینده tDCS در درمان درد
تحریک جریان مستقیم از طریق جمجمه (Transcranial Direct Current Stimulation یا tDCS) به عنوان یک روش تحریک مغناطیسی غیرتهاجمی، توجه زیادی را به عنوان یک استراتژی بالقوه برای تعدیل مدارهای عصبی مرتبط با پروسههای درد مزمن به خود جلب کرده است. وضعیت فعلی استفاده از tDCS در درمان درد، ترکیبی از امیدواری مبتنی بر شواهد اولیه و نیاز مبرم به استانداردسازی و تحقیقات دقیقتر است.
۱. وضعیت کنونی: شواهد و مکانیسمها
tDCS با اعمال یک جریان الکتریکی ضعیف و ثابت از طریق الکترودهای قرار داده شده روی پوست سر، پتانسیل غشای نورونهای قشر مغز را دپولاریزه (تحریک) یا هایپرپولاریزه (مهار) میکند.
مکانیسمهای اصلی اثرگذاری بر درد:
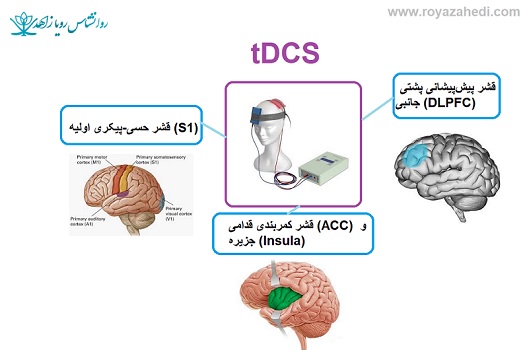
* **قشر حسی-پیکری اولیه (S1):** هدفگیری S1، به ویژه در ناحیه مربوط به قسمت دردناک بدن (مثل دست یا پا)، برای کاهش حس درد سوماتوسنسوری استفاده میشود. الکترود آندال (مثبت) اغلب برای افزایش تحریکپذیری و الکترود کاتدال (منفی) برای کاهش آن به کار میرود.
* **قشر پیشپیشانی پشتی-جانبی (DLPFC):** این ناحیه نقش حیاتی در عملکردهای اجرایی، تنظیم هیجانی و مدولاسیون نزولی درد دارد. تحریک DLPFC میتواند اثرات ضددردی قویتری نسبت به تحریک S1 داشته باشد، زیرا بر جنبههای شناختی-عاطفی درد تأثیر میگذارد.
* **قشر کمربندی قدامی (ACC) و جزیره (Insula):** این نواحی در پردازش عاطفی و ادراکی درد نقش دارند و اهداف نوظهوری در پروتکلهای tDCS محسوب میشوند.
چالشهای کنونی:
* **تغییرپذیری پاسخ:** بزرگترین مانع، نوسان شدید در پاسخ بیماران به درمان است. فاکتورهایی مانند سطح درد اولیه، نوع درد (نوروپاتیک در مقابل نووسیپتیو)، و عوامل فردی مانند ضخامت جمجمه و حجم ماده خاکستری، بر اثربخشی تأثیر میگذارند.
* **عدم استانداردسازی:** پروتکلهای درمانی (مانند شدت جریان، مدت زمان تحریک، و مکانیابی دقیق الکترودها) به طور گستردهای متفاوت هستند، که مقایسه نتایج مطالعات مختلف را دشوار میسازد.
۲. راهبردهای آینده و مسیرهای تحقیق
برای تبدیل tDCS از یک ابزار تحقیقاتی به یک درمان روتین برای درد مزمن، تحقیقات باید بر موارد زیر متمرکز شوند:
الف) درمانهای شخصیسازی شده (Personalized tDCS):
آینده tDCS در گرو **عصبنگاری (Neuroimaging)** است.
۱٫ **نقشهبرداری بر اساس fMRI:** استفاده از تصویربرداری تشدید مغناطیسی کارکردی (fMRI) برای شناسایی دقیق مدارهای عصبی بیشفعال یا کمفعال در هر بیمار مبتلا به درد. این امر امکان هدفگیری دقیقتر ناحیه (مثلاً تحریک DLPFC در بیمارانی با درد با مؤلفه عاطفی بالا و تحریک S1 در کسانی با درد سوماتوسنسوری غالب) را فراهم میکند.
۲٫ **الگوهای تحریک سفارشی:** توسعه الگوریتمهایی که شدت و مدت زمان تحریک را بر اساس ویژگیهای فردی مانند ژنتیک، پاسخهای اولیه به تحریک یا دادههای EEG تنظیم میکنند.
ب) ترکیب با سایر روشها (Combination Therapies):
tDCS به ندرت به عنوان یک درمان منفرد استفاده خواهد شد. راهبردهای مؤثر شامل ترکیب آن با:
* **دارودرمانی:** استفاده از tDCS برای افزایش نفوذپذیری سیناپسی و تقویت اثر داروهایی که به طور معمول برای درد استفاده میشوند (مانند داروهای ضد افسردگی یا شلکنندههای عضلانی).
* **بازتوانی شناختی-رفتاری (CBT):** تحریک مغز همزمان با جلسات CBT میتواند پلاستیسیته مورد نیاز برای تغییر الگوهای تفکر مربوط به درد را افزایش دهد.
ج) بهبود تکنولوژی:
* **tDCS حلقوی و چندالکترودی:** توسعه آرایشهای الکترود پیچیدهتر که امکان تحریک چندین ناحیه مغزی به صورت همزمان یا متوالی را فراهم میکند تا شبکههای درد به طور جامعتری هدف قرار گیرند.
* **دستگاههای خانگی هوشمند:** طراحی دستگاههای tDCS که توسط بیمار در منزل و تحت نظارت مجازی مورد استفاده قرار میگیرد، به شرطی که پروتکلها کاملاً ایمن و با بازخورد آنی باشند.
نتیجهگیری
tDCS پتانسیل بالایی برای ارائه یک راهکار درمانی مقرون به صرفه و کمخطر برای طیف وسیعی از سندرمهای درد مزمن دارد. با این حال، برای تحقق این پتانسیل، جامعه علمی باید بر **استانداردسازی دقیق پروتکلها** و **شخصیسازی درمانها بر اساس نقشهبرداری عصبی اختصاصی بیمار** تمرکز کند.
